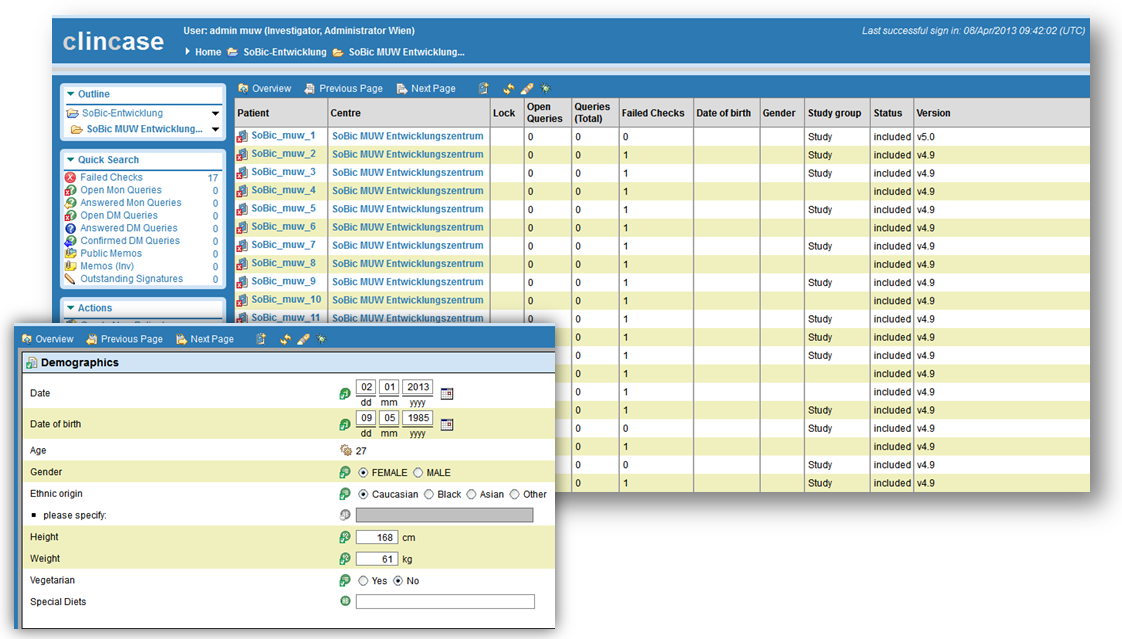
Zur Unterstützung der Kliniker:innen bei der Durchführung akademischer Studien mit Patient:innen wird ein elektronisches Datenerfassungssystem (nach FDA und GCP) angeboten. Die Software "Clincase" der Firma Quadratek ermöglicht eine qualitätsgesicherte Dokumentation von mono- bzw. multizentrischen Studien. Neben der benutzerfreundlichen Web-Oberfläche können die Daten rasch für Auswertungen zur Verfügung gestellt werden.
Wenn Sie einen Eindruck vom System bekommen wollen, können Sie unsere Demo-Studie nutzen. Diese finden Sie unter folgendem Link: https://akimstud.meduniwien.ac.at/clincase/app#
Zugangsdaten:
Username: demo1
Passwort: demo1
Um die Abwicklung Ihrer Studie zu erleichtern, werden vor Beginn der Studie die elektronischen Case Report Forms (eCRF) in "Clincase" umgesetzt. Die Probanden und deren Studiendaten werden in dem System verwaltet und können während und am Ende der Studie für Auswertungen exportiert werden. Nach erfolgreicher Einreichung Ihres Studienprotokolls in der Ethikkomission unterstützen wir Sie bei der elektronischen Umsetzung Ihrer akademischen Studie. Die Studienumsetzung wird auf Ihre Anforderungen abgestimmt, welche vorab in einem persönlichen Beratungsgespräch abgeklärt werden. Aus lizenzrechtlichen Gründen können nur akademische Studien unterstützt werden, wobei eine Erweiterung der Lizenz für industriegesponserte Studien auf Anfrage möglich wäre. Die Kosten dafür werden entsprechend kalkuliert, für akademische Forschungsvorhaben gibt es leistbare Tarife.
Erstgespräch
Wenn Sie bereits ein Studienprotokoll und ein positives Ethikvotum besitzen und die Durchführung Ihrer akademischen Studie finanziell abgesichert ist laden wir Sie gerne zu einem Beratungsgespräch ein, um den Aufwand des Projektes abzuschätzen. Falls Sie einen Antrag auf Förderung stellen, ersuchen wir Sie den Aufwand für die elektronische Studienumsetzung im Ansuchen miteinzubeziehen.
Zu diesem Termin würden wir folgende Informationen benötigen:
- Studienname
- Übergabe des Studienprotokolls
- Ungefährer Zeitplan / Dauer
- Probandenanzahl
- Laufzeit
- Anzahl der User / Anzahl der Zentren
Im Zuge dieses Gesprächs wird das Vorgehen der Studienerstellung von der ersten Umsetzung der Studie im Testsystem bis zur Inbetriebnahme besprochen. Zur Erstellung der elektronischen Studie benötigen wir von Ihnen eine Liste der Variablen in einem Excel, das wir Ihnen per email übermitteln. Danach wird die Studie anhand dieses Excel-Sheets aufgebaut. Nachdem die Studie im Testsystem von Ihnen getestet und alle Änderungswünsche umgesetzt wurden, wird die fertige Studie im Produktivsystem für Ihre Dokumentation bereit gestellt.
Jegliche Änderung im Produktivsystem wird als Change Request behandelt und gespeichert.
Verantwortlichkeiten
Der/die Studienverantwortliche bzw. OEL sichert mit seiner Unterschrift zu, dass folgende Voraussetzungen für die Studie vorhanden sind:
- Genehmigung durch die Ethikkommission
- Finanzierung ist gesichert
- Das erforderliche Personal ist vorhanden
- alle zum Datenschutz erforderlichen Maßnahmen wurden getroffen
- Regelung bei Wechsel der Verantwortlichen
- Regelung bei Studienabbruch bzw. Änderung
Für die Mitarbeiter:innen der MedUni Wien wird ein User mit der MUW-UserID im Studiensystem angelegt und empfehlen daher, falls noch nicht vorhanden, eine MUW - UserID zu beantragen.
Falls Sie kein/e MedUni-Mitarbeiter:in sind und an einer multizentrischen Studie mitwirken, lassen Sie vom Studienarzt einen User für Sie bei uns beantragen.
Das klinische Studiensystem unterstützt multizentrische Studien, da man über das Web die Dateneingabe durchführt.
- Schicken Sie ein Email mit einer kurzen Beschreibung der geplanten Studie.
- Erstgespräch über Ihr Projektvorhaben und das weitere Vorgehen
- Übermittlung des Studienprotokolls
- Anmeldung der Studie bei der Ethik-Kommission.
- Wurde die Studie von der Ethik-Kommission akzeptiert, erstellt der Auftraggeber eine strukturierte Auflistung der gewünschten Variablen/Formulare/Visiten in Excel.
- Umsetzung der eCRFs am Testsystem
- Testmodus der Studie.
- Übernahme der Studie in die Produktionsumgebung.
- Web-Dokumentation der AuftraggeberInnen in der Produktionsumgebung.
Die Rollen für die Studienverantwortlichen können individuell zusammengestellt werden, wobei die Zuteilung der Zugriffsrechte auf Ihre Rolle in der Studie erfolgt. Die gängigsten Rollen sind die des Investigators, des Monitors und des Study Assistants.
Formulare können in einer vordefinierten Abfolge freigeschalten werden. Z.B. erst nach korrekter Eingabe von Inklusions- und Exklusionskriterien werden die weiteren Visiten freigeschalten.
Bevor die Studie in der Produktionsumgebung angelegt wird, wird sie in der Entwicklungsumgebung (Testumgebung) erstellt. Die Entwicklungsumgebung dient den Studienverantwortlichen als Testumgebung um die Studie zu kontrollieren und Änderungswünsche und Verbesserungsvorschläge einzubringen. In der Produktionsumgebung werden die Daten in den elektronischen Formularen bereits dokumentiert und gespeichert.
Ob die Eingabe von Variablen optional oder obligatorisch ist, wird bei der Erstellung der Formulare von Ihnen vor-definiert.
Clincase kann für akademischen Studien, deren Sponsor die Medizinische Universität ist, eingesetzt werden. Das System unterstützt klinische Studien der Phase I-V..
"Clincase" entspricht allen Regularien der FDA (Food and Drug Administration)-Verordnung 21 CFR Part 11 und den international bekannten GCP (Good Clinical Practice) Kriterien. Nachzulesen auf der Clincase-Homepage.
Das Studiensystem lässt sich in zwei unterschiedlichen Umgebungen unter Software öffnen. Je nachdem ob sich die Studie noch im Testmodus befindet oder die Daten bereits erhoben werden, wird die Test- oder Produktionsumgebung gewählt.
"Clincase" ist eine multibrowserfähige Anwendung. Es lässt sich mit den gängigsten Brwosern wie dem Internet Expolorer, Firefox, Chrome usw. öffnen.