Definition
Pulmonale Hypertension (PH) liegt vor, wenn im Lungenkreislauf ein erhöhter Blutdruck besteht. Im Kindesalter ist die PH – wie bei Erwachsenen – übereinkunftsgemäß definiert durch einen pulmonalarteriellen Mitteldruck ≥ 25 mm Hg in Ruhe. Diese Definition setzt eine invasive Messung im Herzkatheter voraus. Die im Alltag gebräuchliche Methode den Druck in der Lunge abzuschätzen ist die Echokardiographie. Liegt eine Trikuspidalinsuffizienz vor, kann der systolische Druck in der Lunge darüber abgeschätzt werden. Ist der gemessene systolische Druck in der Lunge gleich bzw. mehr als 2/3 des Sytemdrucks ist eine Pulmonale Hypertension anzunehmen.
Vorkommen und Pathogenese
PH kommt bei einer Vielzahl von Erkrankungen vor, die unterschiedlichen Formen werden nach der derzeit gültigen Dana Point Klassifikation eingeteilt. Diese Einteilung ist für die kindliche PH nur bedingt anwendbar, da im Kindesalter häufig unterschiedliche Entitäten der Dana Point Klassifikation gleichzeitig auftreten, das 2011 in Panama gegründete Konsensus Papier berücksichtigt die Vielfalt und Besonderheiten der kindlichen PH in der Einteilung.
Trotz der Verschiedenheit der PH Formen scheinen drei Hauptfaktoren für den erhöhten Widerstand im pulmonalen Kreislauf verantwortlich zu sein: Vasokonstriktion (Gefäßengerstellung), Remodelling der pulmonalen Gefäßwand und Thrombose (Gerinnselbildung) in situ.
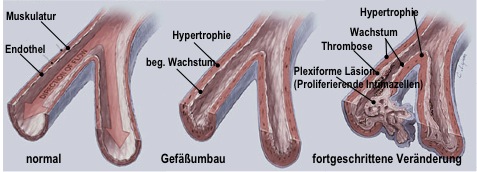
Pathogenetisch entscheidend ist dabei eine endotheliale Dysfunktion, die sich über unterschiedliche Noxen, wie Hypoxie, mechanische Läsion (shear stress), Inflammation oder vor dem Hintergrund einer genetischen Disposition aber auch über noch ungeklärte Mechanismen entwickeln kann. Dadurch liegt eine Störung der normalen Balance zwischen Vasodilatatoren (gefäßerweiternde Substanzen) und Vasokonstriktoren (gefäßverengende Substanzen), zwischen Wachstums-Inhibitoren und mitogenen Faktoren und zwischen antithrombotischen und prothrombotischen Determinanten vor. Histologisch besteht dadurch das einheitliche Bild eines obliterativen vaskulären Remodellings der Lungenarterien. Konzentrische Intimaverdickung, Hypertrophie der Media, sowie Fibroblastenproliferation der Adventitia, Thromben in den kleinen Pulmonalgefäßen, und schliesslich sogenannten „plexiforme Läsionen“ - das sind kleine glomerulum-artige Gefäßballen, stellen ein für alle PH Formen in mehr oder weniger starker Ausprägung vorhandenes Muster dar. (s.h. Abb1)
Klinik und Diagnostik
Ähnlich wie bei Erwachsenen stellt auch im Kindesalter die Kurzatmigkeit bei körperlicher Belastung ein sehr frühes Symptom dar. Diese ist jedoch unspezifisch und wird oft als fehlende körperliche Fitness oder Asthma bronchiale interpretiert. Fortgeschrittenere Symptome sind Thoraxschmerz, verminderte Belastbarkeit, Schwindel und Synkopen. Letztere sind Folge der eingeschränkten Fähigkeit das Herzzeitvolumen und damit auch das Sauerstoffangebot an die Organe unter Belastung zu steigern. Nicht selten wird bei Kindern mit Synkopen die Fehldiagnose eines cerebralen Anfallsleiden gestellt.
Eine verspätete Diagnosestellung mit einer Latenz von derzeit im Mittel 2 Jahren ist damit nicht selten. Allerdings ist das Bewusstsein für diese Erkrankung in den letzten Jahren gestiegen. Damit kann trotz der unspezifischen Symptomatik eine gründliche physikalische Untersuchung mit genauer Erhebung der Familienanamnese bereits Grundlage für eine Verdachtsdiagnose sein.
Interessant erscheint die Erfahrung, dass bei Kindern im Gegensatz zu Erwachsenen eine deutliche Diskrepanz zwischen ermittelten pulmonalarteriellen Druckwerten und klinischer Symptomatik besteht. Kinder haben zum Zeitpunkt der Diagnosestellung meist deutlich höhere Druckwerte im kleinen Kreislauf als Erwachsene.
Zur Diagnosesicherung werden von nationalen und internationale Gesellschaften folgende Untersuchungen empfohlen: 12 Kanal EKG, Lungenröntgen, transthorakale Echokardiographie und Herzkatheteruntersuchung. Zur Differentialdiagnose der vielfältigen Ursachen bedarf es einer Lungenfunktionstestung, einer arteriellen Blutgasanalyse mit anschließender pulsoxymetrischer Sauerstoffsättigung über 24 Stunden, eventuell einer Schlaflaboruntersuchung, sowie einer Ventilations/Perfusionsszintigraphie.
Je nach Befundkonstellation sind zur weiteren Abklärung verschiedene hochspezialisierte Untersuchungsmethoden (z.B. cardiales MRI, HRCT, Multislice CT, Pulmonalisangiographie) anzuwenden.
Ziel der Diagnostik ist neben der exakten Klassifikation der PH auch die Festlegung des Schweregrades der Erkrankung mit NYHA Klassifizierung, was im Kindesalter schwierig ist.
Zur Abschätzung der Belastbarkeit dient die Spiroergometrie bzw. der 6 Minuten Gehtest, letzterer ist etwa ab dem 4. Lebensjahr möglich.
Unter den diagnostischen Untersuchungsverfahren spielt die Herzkatheteruntersuchung eine entscheidende Rolle. Sie erlaubt neben der exakten Ermittlung der Druck und Widerstandverhältnisse die Prüfung der Reagibilität des Lungengefäßbetts. Die Messergebnisse dienen dabei einerseits zur Festlegung der medikamentösen Therapie. Andererseits kann dadurch bei Kindern mit PH infolge von Herzfehlern über Operabilität entschieden werden. Bei Kindern mit schwerer nicht operabler Herzerkrankung dienen die Messergebnisse der Entscheidung ob eine Herztransplantation möglich ist.
Bei größeren Kindern kann die Herzkatheteruntersuchung unter lokaler Betäubung ohne Sedierung durchgeführt werden, bei kleineren oder nicht kooperierenden Kindern erfolgt sie mit Analgosedierung.
Therapie
Supportive Massnahmen:
Alle therapeutischen Maßnahmen zielen darauf ab, eine zusätzliche Gefäßkonstriktion durch Hypoxie (Sauerstoffabfall) oder Hyperkapnie (Kohlendioxidanstieg) zu vermeiden und einen verbesserten pulmonalen Blutfluss zu erreichen.
Supportive Therapien sind alle Maßnahmen außer den spezifischen Vasodilatatoren, das heißt orale Antikoagulation, Glykoside, Diuretika aber auch körperliche Schonung und Sauerstoffgabe bei Sättigungen unter 93%-90%.
Da eine verminderte alveoläre Sauerstoffkonzentration zu einer zusätzlichen pulmonalen Vasokonstriktion führt, sollten entsprechende Situationen, wie beispielsweise Aufenthalte in größerer Höhe oder Flugreisen gemieden werden oder nur unter kontinuierlicher Sauerstoffzufuhr (z.B. O2 Maske beim Fliegen) erfolgen.
Generell wird für Kinder mit PH eine Pneumokokken, RSV und Influenza Impfung empfohlen, inklusive einer Umgebungsprophylaxe der Familienmitglieder.
Pulmonale Infekte sollten großzügig, eventuell auch unter stationären Bedingungen und mit zusätzlicher Sauerstoffgabe behandelt werden, dazu gehört auch eine konsequente Fiebersenkung und eventuell Rehydrierung, da durch den erhöhten Stoffwechsel im Fieber eine metabolische Azidose die pulmonale Hypertension verstärken kann.
Ein akuter Flüssigkeitsverlust wie zum Beispiel bei einer schweren Magen Darm Grippe muss konsequent ausgeglichen werden, da der vorlastabhängige rechte Ventrikel sonst mit akutem Abfall des Herzzeitvolumens reagieren kann.
Mädchen und junge Frauen sollte hinsichtlich einer adäquaten Kontrazeption entsprechend aufgeklärt werden, da Schwangerschaft und Entbindung mit einem hohen Risiko verbunden sind (Mortalität 30-50%).
Vasoaktive Therapie
Das Behandlungskonzept beruht auf dem zunehmenden Verständnis dass die PH Folge einer fortschreitenden Gefäßerkankung ist, die durch Proliferation (Wachstum), Inflammation (Entzündung) und Vasokonstriktion (Gefäßengerstellung) zu einer zunehmenden Verstopfung der Gefäße führt. Die Behandlungsalgorithmen zielen darauf ab diese Komponenten der Gefäßobstruktion zu beeinflussen.
Die angewendeten Substanzen bewirken Hemmung der Vasokonstriktion durch pharmakologische Vasodilatation sowie Verlangsamung der strukturellen Gefäßumbauprozesse durch antinflammatorische und antiproliferative Effekte („Anti Remodelling Strategie“).
Kalziumkanalblocker
Diese sehr heterogene Gruppe von Substanzen verhindert den Kalziumeinstrom durch die langsamen Kalziumkanäle von Herz- und glatten Muskelzellen, an den Lungengefäßen komme es dadurch zu Vasodilatation.
Kalziumkanalblocker werden bei Patienten, mit Responderstatus - das heisst Patienten deren Gefäßreagibilität bei der Herzkatheteruntersuchung erhalten ist – gegeben.
Im Langzeitverlauf profitiert nur etwa die Hälfte der hämodynamischen Responder - Kinder von hochdosierten Kalzium Antagonisten als Monotherapie. Daher bedarf es einer strengen Therapieüberwachung mit regelmäßiger Reeavaluierung der Gefäßreagibilität im Herzkatheter.
Prostazykline

Die Mediierung der Vasodilatation erfolgt durch die Aktivierung von spezifischen PGI2-Membranrezeptoren, die an das Adenylat-und Guanylatzyklasesystem gekoppelt sind. Andere Wirkungen, ebenfalls von spezifischen Rezeptoren mediiert, beinhalten die Inhibierung der Plättchenaktivierung und –aggregation, aber auch die Adhäsion von Leukozyten an Endothelzellen. Die Einführung der Prostazyklintherapie in den 80er Jahren hat das Überleben von PH Patienten deutlich gebessert.
Prostazyklin hat eine Halbwertszeit von 3 Minuten und muss daher parenteral, also intravenös verabreicht werden. Um eine kontinuierliche und sichere Zufuhr zu gewährleisten, muß ein zentralvenöser Gefäßzugang gesetzt werden, die Substanz (Flolan® ) wird über eine Pumpe, welche die Patienten in einem Rucksack mit sich tragen, infundiert (s.h. Abb.). Aufgrund der Instabilität der Substanz wird das Medikament täglich frisch zubereitet. Diese Therapieform ist sehr aufwendig und mit einem hohen Risiko (Katheterinfektion, Thrombose) verbunden und erfordert daher eine eingehende Beratung, Einschulung und Unterstützung der Patienten und der Eltern betroffener Kinder.
Das Prostazyklin Derivat Iloprost (Ilomedin®) ist im Hinblick auf Licht und Temperaturempfindlichkeit stabiler und hat eine längere Halbwertszeit von 30 min. Im Vergleich zu Flolan® und bietet es daher Vorteile in der intravenösen Handhabung.
Iloprost (Ventavis®) kann auch inhalativ eingesetzt werden, aufgrund der Wirkdauer sind etwa 6-12 Inhalationen pro Tag notwendig.
Treprostinil (Remodulin®), eine anderes Prostazyklinanalogon kann intravenös oder subkutan verabreicht werden, aufgrund der Nebenwirkungen (lokale Schmerzen, Schwellungen) hat sich diese Darreichungsform bei Kindern nicht bewährt.
Bosentan
Mit Bosentan (Tracleer®) steht der erste am Markt zugelassene duale Endothelin-Rezeptor-Antagonist (ERA) für die orale Behandlung der PH zur Verfügung. Endothelin wird bei der PH vermehrt gebildet und fördert die Vasokonstriktion und das Remodelling der Pulmonalgefäße durch Bindung an Endothelinrezeptoren (ET-A- und ET-B-Rezeptoren). Bosentan kombiniert mit der Blockade des ET-A- und ET-B-Rezeptors vasodilatatorische mit antiinflammatorischen und antifibrotischen Wirkungen.
Entsprechend der Richtlinien ist Bosentan bei PH mit Non Responderstatus (ohne erhaltene Gefäßreagibilität) indiziert. Mittlerweile ist die Wirksamkeit dieses Medikaments auch bei Kindern gut untersucht. Bosentan ist gut verträglich und sicher und wird 2x täglich eingenommen. Regelmäßge Kontrollen der Leberparameter werden jedoch aufgrund des Nebenwirkungsprofils empfohlen.
Ambrisentan ist ein selektiver Endothelin A-Rezeptorantagonisten und ist derzeit in Europa nur bei Erwachsen zugelassen.
Sildenafil
Sildenafil (Revatio®) ist ein Phosphodiesterasehemmer und hemmt den Abbau von zyklischem Guanosin-Monophosphat (cGMP), dieses wird durch endogenes NO vermehrt intrazellulär freigesetzt und führt zur Vasodilatation. Sildenafil verstärkt somit die NO Wirkung und hat zudem auch antiproliferative Effekte. In der Therapie der PH hat es einen festen Stellenwert und ist seit 2011 auch bei Kindern mit PH in Österreich zugelassen. Sildenafil wird bei Non Responderstatus eingesetzt und wird prinzipiell gut vertragen. Sildenafil wird 3-4 x täglich verabreicht, gelegentlich in sehr speziellen Fällen- ist auch eine häufigere Einnahme notwendig.
Bei Kindern kann es zu Beginn gelegentlich zu Flush (Erröten), Kopfschmerzen und Blutdruckabfall kommen, diese Nebenwirkungen sind allerdings dosisbahängig und können in der Regel durch vorsichtiges Einschleichen des Medikaments weitgehend vermieden werden.
Tadalafil, ein länger wirksamer Phosphodieesterasehemmer, ist derzeit nur bei Erwachsenen zugelassen.
Kombinationstherapien und andere Maßahmen
Die obengenannten Therapien werden individuell entsprechend der PH Form, des Schweregrads der Erkrankung und der hämodynamisch ermittelten Werte eingesetzt.
Nachdem diese Therapien über unterschiedliche Mechanismen wirken ist die Kombination dieser Präparate sinnvoll und hat sich auch im klinischen Alltag bewährt, da dadurch gleichzeitig verschiedene Mechanismen die den Gefäßumbau in Gang setzen und vorantreiben, angegriffen werden.
Bei zunehmender Rechtsherzinsuffizienz oder Auftreten von Synkopen kann die Durchführung einer Atrioseptektomie hilfreich sein. Mittels Herzkatheter wird dabei ein kleiner Vorhofseptumdefekt erzeugt, damit entsteht eine Art „Überdruckventil“ auf Vorhofebene. Das Vorliegen einer solchen kleinen interatrialen Kommunikation hat präventiven Charakter im Hinblick auf ein akutes Rechtsherzversagen bzw auf ein „low cardiac output“ Syndrom, allerdings unter Inkaufnahme einer Untersättigung durch den R/L Shunt.
Ausblick und Zusammenfassung
Mit zunehmender Erforschung der komplexen Mechanismen die bei der Entwicklung dieser Gefäßerkrankung involviert sind, wurden in den letzten Jahren weitere Angriffsorte und damit Therapieansätze entsprechend der Anti Remodelling Strategie entdeckt, dazu gehören Rho Kinase Inhibitoren oder auch Tyrosinkinasehemmer wie beispielweise Imatinib ( Gleevec®) beide sind derzeit in klinischer Erprobung.
Das Verständnis dieser Erkrankung und der Einsatz der neuen Medikamente haben den Kindern mit PH völlig neue Perspektiven eröffnet. Sowohl Lebensqualität als auch Prognose haben sich in den letzten beiden Jahrzehnten deutlich gebessert.
Trotzdem bleibt die PH eine fortschreitende Erkrankung, die zu einem Rechtsherzversagen führt. In den meisten Fällen kann trotz der medizinischen Fortschritte keine echte Heilung erzielt werden, sondern nur eine Verlangsamung ihres Fortschreitens.
Nach Ausschöpfen aller medikamentösen und interventionellen Maßnahmen stellt schließlich die Lungen bzw. Herz- Lungentransplantation die letzte therapeutische Option dar. Auch hier haben sich die Überlebenschancen dank technischer Entwicklungen und neuer Therapieansätze in den letzten Jahren gebessert.
Aktualisierte klinische Klassifikation der Pulmonalen Hypertension nach Dana Point 2008
Die Screening Karte für Pulmonale Hypertension finden Sie HIER